AG Ishikawa-Ankerhold
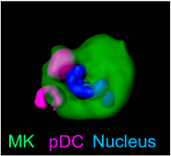
Mechanismen der Thrombozytenbiogenese und ihre Auswirkungen auf die Immunthrombose unter Verwendung der Intravitalmikroskopie
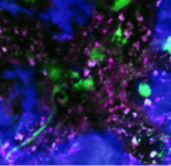
Die Intravitalmikroskopie (IVM) ist die Methode der Wahl für die direkte Beobachtung dynamischer zellulärer Prozesse in lebenden Organismen. Das primäre Ziel besteht darin, die Interaktionen zwischen Zellen in Geweben und Organen in ihrer natürlichen Umgebung zu untersuchen, sowohl unter normalen physiologischen Bedingungen als auch in Krankheitsmodellen. Dieser Ansatz liefert einzigartige Erkenntnisse, die mit keiner anderen Methode bei vergleichbarer räumlicher und zeitlicher Auflösung erzielt werden können.
Die hochauflösende Beobachtung zellulärer Mikroumgebungen in lebenden Organismen stellt verschiedene technologische, präparative und methodische Herausforderungen dar. Um diesen zu begegnen, setzen wir modernste 4D-In-vivo-Bildgebungstechniken ein, darunter konfokale Laserscanning- und Multiphotonenmikroskopie, kombiniert mit fortschrittlicher Software zur Live-Driftkorrektur (VivoFollow-Software 7,12), um Bewegungsartefakte, die durch Atmung und Herzaktivität verursacht werden, zu korrigieren oder zu minimieren.
Über die Entwicklung der erforderlichen technologischen und methodischen Rahmenbedingungen hinaus haben wir auch eine Reihe von Mausmodellen etabliert, die aufgrund ihrer genetischen Ähnlichkeit mit dem Menschen die Untersuchung menschlicher Krankheitsmuster und die Entwicklung geeigneter therapeutischer Ansätze erleichtern.
Unsere Forschung spielte eine zentrale Rolle im Rahmen des Sonderforschungsbereichs (SFB) 914, der sich mit der Migration von Immunzellen bei Entzündungen, Entwicklung und Krankheiten befasste. Dort stellten wir eine Kernkompetenzplattform für die 4D-Multiphotonen-Intravitalmikroskopie des Immunzelltransports in Mausmodellen bereit. Im SFB 1321, der sich mit der Modellierung und Bekämpfung von Bauchspeicheldrüsenkrebs befasst, konzentriert sich unsere Arbeit auf die Untersuchung von Mechanismen, die die Gerinnung und Thrombose während der Metastasierung fördern. Darüber hinaus beteiligen wir uns an zahlreichen Kooperationsprojekten, darunter dem SFB 1123, der sich mit Atherosklerose und neuen therapeutischen Ansatzpunkten befasst.
Ein wichtiger Schwerpunkt unserer Forschungsgruppe ist die Untersuchung der Immunthrombose, insbesondere der Mechanismen, die die Thrombozytenbiogenese im Knochenmark regulieren, und deren Auswirkungen auf thromboinflammatorische Erkrankungen. In diesem Zusammenhang haben wir kürzlich einen wichtigen Regulationsmechanismus der Megakaryopoese entdeckt, bei dem plasmazytoide dendritische Zellen Interferon-alpha freisetzen und so die Thrombozytenproduktion beeinflussen. Diese bahnbrechende Entdeckung, die in Nature 5 (2024) veröffentlicht wurde, wurde durch den Einsatz von IVM ermöglicht und unterstreicht die Leistungsfähigkeit dieser Technologie bei der Aufdeckung von Zellinteraktionen in vivo. Das Verständnis dieses Mechanismus liefert neue Erkenntnisse über die Rolle der Immunregulation bei der Thrombozytenbildung und ihren möglichen Beitrag zu immunthrombotischen Ereignissen.
Unsere Forschungsgruppe widmet sich sowohl der Weiterentwicklung und Standardisierung von Intravitalmikroskopietechniken als auch der Entwicklung hochinformativer Mausmodelle (Link zur IVM-Webseite). Unser wissenschaftlicher Schwerpunkt umfasst die Herz-Kreislauf-Forschung, Immunthrombose-Prozesse sowie die zelluläre Dynamik und Interaktionen von Immunzellen mit Krankheitserregern, Krebszellen und innerhalb der Embryonalentwicklung.
Ein wesentlicher Vorteil unserer Arbeit ist ihre enge Verbindung zu klinischen Anwendungen. An der Schnittstelle zwischen Grundlagenforschung und klinischer Medizin angesiedelt, zielen unsere Studien darauf ab, die Lücke zwischen wissenschaftlichen Entdeckungen und medizinischen Innovationen zu schließen.
Methoden
Die Expertise von AG Ishikawa-Ankerhold umfasst eine breite Palette von translationalen Mausmodellen für Krankheiten, die verschiedene Gewebe und Organe abdecken, darunter Haut, Leber, Magen, Niere, Milz, Bauchspeicheldrüse, Plazenta, Dottersack, Gehirn, Fettgewebe, Knochen und Knochenmark, Darm und Muskelgewebe (Abbildung 1).

Abbildung 1. Multiphotonen-Intravitalbildgebung von Mausgeweben. Repräsentative Intravital-Multiphotonenmikroskopie-Bilder (IVM) verschiedener Mausorgane, darunter Gehirn, Knochenmark, Leber, Magen, Bauchspeicheldrüse und Dottersack. Die Bilder zeigen Immunzellen, Tumorzellen und Blutgefäße, die mithilfe von Fluoreszenzmarkern sichtbar gemacht wurden. Diese Technik ermöglicht die Echtzeitverfolgung der Zelldynamik und erleichtert die Beobachtung therapeutischer Eingriffe in vivo. Verschiedene Farben stehen für unterschiedliche Strukturen oder Zelltypen und helfen bei der Untersuchung gewebespezifischer Interaktionen und des Krankheitsverlaufs.
Um diese Modelle mit hoher räumlicher und zeitlicher Auflösung zu untersuchen, setzen wir modernste intravitale Bildgebungstechniken ein, wobei der Schwerpunkt auf der 4D-Multiphotonenmikroskopie und der konfokalen Laserscanning-Mikroskopie liegt. Diese Technologien ermöglichen es uns, dynamische zelluläre Prozesse in vivo mit beispielloser Präzision zu erfassen.
Neben fortschrittlicher Bildgebung umfasst unser methodisches Spektrum:
Fortschrittliche intravitale Bildgebungstechniken unter Verwendung von 4D-konfokaler Laserscanning- und Multiphotonenmikroskopie (Link zur IVM-Webseite)
- 3D-Drucktechnologien zur individuellen Anpassung von Probenhaltern, um eine optimale Positionierung und Stabilität während der Bildgebung zu gewährleisten
- Bildanalyse (Imaris-, ZEN- und Fiji-Software), mehrdimensionale Bildverarbeitung und Bildrekonstruktion, um ein tieferes Verständnis komplexer biologischer Strukturen und Interaktionen zu ermöglichen
- Immunhistochemische/Immunfluoreszenz-Charakterisierung von Geweben und Zelltypen sowie Verwendung von Lebendzellfarbstoffen zur Visualisierung spezifischer biologischer Prozesse
- Durchflusszytometrische Charakterisierung und Trennung verschiedener Zellpopulationen, was gezielte Analysen und Funktionsstudien ermöglicht
- Zellmigrations- und Chemotaxis-Assays unter Verwendung von Durchflusskammern, mit denen wir die gerichtete Bewegung von Zellen als Reaktion auf verschiedene Reize untersuchen können
Durch die Integration dieser fortschrittlichen Methoden wollen wir Krankheitsmodelle verfeinern, die Bildgebungsgenauigkeit verbessern und zu einem tieferen Verständnis des Zellverhaltens sowohl bei gesunden als auch kranken Menschen beitragen.
Publications (selected) *equal contribution
1. Bodogai M, Park B, Braikia FZ, Naqing F, Kumaraswami K, Chen C, Ragonnaud E, Stack S, Ormanns S, Günther M, Ishikawa-Ankerhold H, De S, Ferrucci L, Sen R, Duren Z, Beerman I, Biragyn A. (2025). A distinct population of CD8+ T cells expressing CD39 and CD73 accumulates with age and supports cancer progression. Nat Aging. 2025 Oct;5(10):2055-2069. doi: 10.1038/s43587-025-00966-3
2. Papargyriou A, Najajreh M, Cook DP, Maurer CH, Bärthel S, Messal HA, Ravichandran SK, Richter T, Knolle M, Metzler T, Shastri AR, Öllinger R, Jasper J, Schmidleitner L, Wang S, Schneeweis C, Ishikawa-Ankerhold H, Engleitner T, Mataite L, Semina M, Trabulssi H, Lange S, Ravichandra A, Schuster M, Mueller S, Peschke K, Schäfer A, Dobiasch S, Combs SE, Schmid RM, Bausch AR, Braren R, Heid I, Scheel CH, Schneider G, Zeigerer A, Luecken MD, Steiger K, Kaissis G, van Rheenen J, Theis FJ, Saur D, Rad R, Reichert M. (2025). Heterogeneity-driven phenotypic plasticity and treatment response in branched-organoid models of pancreatic ductal adenocarcinoma. Nat Biomed Eng. 2024 Dec 10. doi: 10.1038/s41551-024-01273-9. Online ahead of print.PMID: 39658630.
3. Blobner J, Dengler L, Eberle C, Herold JJ, Xu T, Beck A, Mühlbauer A, Müller KJ, Teske N, Karschnia P, van den Heuvel D, Schallerer F, Ishikawa-Ankerhold H, Thon N, Tonn JC, Subklewe M, Kobold S, Harter PN, Buchholz VR, von Baumgarten L. (2024). PD-1 blockade does not improve efficacy of EpCAM-directed CAR T-cell in lung cancer brain metastasis. Cancer Immunol Immunother. 2024 Oct 3;73(12):255. doi: 10.1007/s00262-024-03837-9.
4. Ishikawa-Ankerhold H, Busch B, Bader A, Maier-Begandt D, Dionisio F, Namineni S, Vladymyrov M, Harrison U, van den Heuvel D, Tomas L, Walzog B, Massberg S, Schulz C, Haas R. (2024). Novel multiphoton intravital imaging enables real-time study of Helicobacter pylori interaction with neutrophils and macrophages in the mouse stomach. PLoS Pathog. 2024 Sep 30;20(9):e1012580. doi: 10.1371/journal.ppat.1012580.
5. Wang X, Campbell B, Bodogai M, McDevitt RA, Patrikeev A, Gusev F, Ragonnaud E, Kumaraswami K, Shirenova S, Vardy K, Alameh MG, Weissman D, Ishikawa-Ankerhold H, Okun E, Rogaev E, Biragyn A. (2024). CD8+ T cells exacerbate AD-like symptoms in mouse model of amyloidosis. Brain Behav Immun. 2024 Nov;122:444-455. doi: 10.1016/j.bbi.2024.08.045. Epub 2024 Aug 25.
6. Gaertner F, Ishikawa-Ankerhold H*, Stutte S, Fu W, Weitz J, Dueck A, Nelakuditi B., Fumagalli V., Van den Heuvel D, Belz L., Sobirova G., Zhang Z, Titova A., Martinez Navarro A., Pekayvaz K., Lorenz M, von Baumgarten L, Jan Kranich, Tobias Straub, Bastian Popper, Vanessa Zheden, Walter Anton Kaufmann, Chenglong Guo, Piontek G., von Stillfried S., Boor P, Colonna M., Clauß S., Schulz C., Brocker T., Walzog B, Scheiermann C., C. Aird W., Nerlov C., Stark K., Petzold T., Engelhardt S., Sixt M., Hauschild R., Rudelius M., Oostendorp R. A. J., Iannacone M., Heinig M., Massberg S. (2024). Plasmacytoid dendritic cells control homeostasis of megakaryopoiesis. NATURE 631:645–653 (2024). https://doi.org/10.1038/s41586-024-07671-y.
7. Mueller T, Pilartz M, Thakur M, LangHeinrich T, Luo J., Block R., Hoeflinger J. K. L, Sarah M., Karaj F., Garcia P. L., Öllinger R., Engleitner T., Thoss J., Voelkl M., Tersteeg C., Koedel U., Zigman K. A., Teupser D., Wygrecka M., Ye H., T Preissner K., Radbruch H., Elezkurtaj S., Mack M., Von Hundelshausen P., Weber C., Massberg S., Schulz C., Rad R., Huber S., Ishikawa-Ankerhold H* and Bernd E*. (2024). Mutual regulation of CD4+ T cells and intravascular fibrin in infections. Haematologica, 2024, 109:2487-2499. doi: https://doi.org/10.3324/haematol.2023.284619.
8. Liu H, Ishikawa-Ankerhold H*, Winterhalter J, Lorenz M, Vladymyrov M, Massberg S, Schulz C, and Orban M. (2023) Multiphoton In Vivo Microscopy of Embryonic Thrombopoiesis Reveals the Generation of Platelets through Budding. Cells 2023, 12(19), 2411; https://doi.org/10.3390/cells12192411
9. Petzold T, Zhang Z, Ballesteros I, Saleh I, Polzin A, Thienel M, Liu L, Ul Ain Q, Ehreiser V, Weber C, Kilani B, Mertsch P, Götschke J, Cremer S, Fu W, Lorenz M, Ishikawa-Ankerhold H, Raatz E, El-Nemr S, Görlach A, Marhuenda E, Stark K, Pircher J, Stegner D, Gieger C, Schmidt-Supprian M, Gaertner F, Almendros I, Kelm M, Schulz C, Hidalgo A, Massberg S. (2022) Neutrophil "plucking" on megakaryocytes drives platelet production and boosts cardiovascular disease. Immunity. Oct 18:S1074-7613(22)00542-8. doi: 10.1016/j.immuni.2022.10.001.
10. Ishikawa-Ankerhold H, Kroll J, Heuvel DVD, Renkawitz J, Müller-Taubenberger A. (2022) Centrosome Positioning in Migrating Dictyostelium Cells. Cells. May 29;11(11):1776. https://doi: 10.3390/cells11111776.
11. S. Stutte, H. Ishikawa-Ankerhold, L. Lynch, S. Eickhoff, S. Nasiscionyte, C. Guo, D. van den Heuvel, D. Setzensack, M. Colonna, D. Maier-Begandt, L. Weckbach, T. Brocker, Chr. Schulz, B. Walzog & U. von Andrian. (2022) High-fat diet rapidly modulates the homeostatic phenotype and function of plasmacytoid dendritic cells and alters their trafficking in adipose tissue. J Immunol. 2022 Mar 15;208(6):1445-1455. doi: 10.4049/jimmunol.2100022. Epub 2022 Feb 18.
12. Weckbach LT, Schweizer L, Kraechan A, Bieber S, Ishikawa-Ankerhold H, Hausleiter J, Massberg S, Straub T, Klingel K, Grabmaier U, Zwiebel M, Mann M, Schulz C; EMB Study Group. (2022) Association of Complement and MAPK Activation With SARS-CoV-2 Associated Myocardial Inflammation. AMA Cardiol. 2022 Mar 1;7(3):286-297. doi: 10.1001/jamacardio.2021.5133.
13. Lasch M, Vladymyrov M, van den Heuvel D, Götz P, Deindl E, Ishikawa-Ankerhold H. (2021) Multiphoton intravital imaging as a tool for monitoring leukocyte recruitment during arteriogenesis in vivo in a murine hindlimb model. J Vis Exp. 2021 Sep 30:(175). DOI: 10.3791/62969.
14. Zhang W, Karschnia P, von Mücke-Heim IA, Mulazzani M, Zhou X, Blobner J, Mueller N, Teske N, Dede S, Xu T, Thon N, Ishikawa-Ankerhold H, Straube A, Tonn JC, von Baumgarten L. (2021) In vivo two-photon characterization of tumor-associated macrophages and microglia (TAM/M) and CX3CR1 during different steps of brain metastasis formation from lung cancer. Neoplasia. 2021 Nov;23(11):1089-1100.
15. Nicolai L, Kaiser R, Escaig R, Hoffknecht ML, Anjum A, Leunig A, Pircher J, Ehrlich A, Lorenz M, Ishikawa-Ankerhold H, Aird WC, Massberg S, Gaertner F. (2021) Single platelet and megakaryocyte morpho-dynamics uncovered by multicolor reporter mouse strains in vitro and in vivo. Haematologica. 2021 Sep 16.
16. Stutte S, Ruf J, Kugler I, Ishikawa-Ankerhold H, Parzefall A, Marconi P, Maeda T, Kaisho T, Krug A, Popper B, Lauterbach H, Colonna M, von Andrian U, Brocker T. (2021) Type I interferon mediated induction of somatostatin leads to suppression of ghrelin and appetite thereby promoting viral immunity in mice. Brain Behav Immun. Jul; 95:429-443.
17. Lasch M, Kumaraswami K, Nasiscionyte S, Kircher S, van den Heuvel D, Meister S, Ishikawa-Ankerhold H*, Deindl E*. (2020) RNase A Treatment Interferes With Leukocyte Recruitment, Neutrophil Extracellular Trap Formation, and Angiogenesis in Ischemic Muscle Tissue. Front Physiol. Nov 6, 11: 576736.
18. Weinberger T, Esfandyari D, Messerer D, Percin G, Schleifer C, Thaler R, Liu L, Stremmel C, Schneider V, Vagnozzi RJ, Schwanenkamp J, Fischer M, Busch K, Klapproth K, Ishikawa-Ankerhold H, Klösges L, Titova A, Molkentin JD, Kobayashi Y, Engelhardt S, Massberg S, Waskow C, Perdiguero EG, Schulz C. (2020) Ontogeny of arterial macrophages defines their functions in homeostasis and inflammation. Nat Commun. Sept 11, 11: 4549.
19. Stocker TJ, Pircher J, Skenderi A, Ehrlich A, Eberle C, Megens RTA, Petzold T, Zhang Z, Walzog B, Müller-Taubenberger A, Weber C, Massberg S, Ishikawa-Ankerhold H*, Schulz* C. (2018). The Actin Regulator Coronin-1A Modulates Platelet Shape Change and Consolidates Arterial Thrombosis. Thromb Haemost. Dec; 118(12):2098-2111.
20. Pircher J, Czermak T, Ehrlich A, Eberle C, Gaitzsch E, Margraf A, Grommes J, Saha P, Titova A, Ishikawa-Ankerhold H, Stark K, Petzold T, Stocker T, Weckbach LT, Novotny J, Sperandio M, Nieswandt B, Smith A, Mannell H, Walzog B, Horst D, Soehnlein O, Massberg S, Schulz C. (2018). Cathelicidins prime platelets to mediate arterial thrombosis and tissue inflammation. Nat Commun. Apr 18; 9 (1): 1523.
21. Stremmel C, Schuchert R, Wagner F, Thaler R, Weinberger T, Pick R, Mass E, Ishikawa-Ankerhold H, Margraf A, Hutter S, Vagnozzi R, Klapproth S, Frampton J, Yona S, Scheiermann C, Molkentin JD, Jeschke U, Moser M, Sperandio M, Massberg S, Geissmann F, Schulz C. (2018). Yolk sac macrophage progenitors traffic to the embryo during defined stages of development. Nat Commun. Jan 8; 9 (1): 75.
22. Gaertner F, Ahmad Z, Rosenberger G, Fan S, Nicolai L, Busch B, Yavuz G, Luckner M, Ishikawa-Ankerhold H, Hennel R, Benechet A, Lorenz M, Chandraratne S, Schubert I, Helmer S, Striednig B, Stark K, Janko M, Böttcher RT, Verschoor A, Leon C, Gachet C, Gudermann T, Mederos Y Schnitzler M, Pincus Z, Iannacone M, Haas R, Wanner G, Lauber K, Sixt M, Massberg S. (2017). Migrating platelets are mechano-scavengers that collect and bundle bacteria. Cell. Nov 30; 171 (6): 1368-1382.e23.
23. Stocker TJ, Ishikawa-Ankerhold H, Massberg S, Schulz C (2017). Small but mighty: Platelets as central effectors of host defense. Thromb Haemost. Apr 3;117(4):651-661. doi: 10.1160/TH16-12-0921. Epub 2017 Feb 16
24. Schulz C, Petzold T, Ishikawa-Ankerhold H. (2021) Macrophage regulation of granulopoiesis and neutrophil functions. Antioxid Redox Signal. Oct 27. doi: 10.1089/ars.2020.8203. PMID: 33107319. Review
Book chapters
Förderungen
Promotion of Women Scientists
Project title: Mechanisms regulating splenic platelets biogenesis in sepsis and its implications for cardiovascular diseases
2025 -2027
FöFoLe (Förderprogramm für Forschung und Lehre des Medizinischen Dekanats)-Promotionsprojekt
Project title: Investigating the Role of Plasmacytoid Dendritic Cells in Immune-Primed Platelet Formation in Thromboinflammation
2026 -2027

PD Dr. rer. nat. Hellen Ishikawa-Ankerhold
AG Leiterin und Leiterin der Multiphoton Intravital Mikroskopie
Larissa Belz, M. Sc.
PhD student
Gulnoza Sobirova
MD student
Maximilian Seeberger
MD
Yinfeng Zhu
PhD student
Qiongjie Ding
PhD student
Jinlong Wan
PhD student
Paulina Luna David
Med Studentin

Dominic van den Heuvel
technischer Assistent – Lichtmikroskopie und Bildanalyse
Sanjana Balaji
Student assistant



